前沿医疗 | “吃屎”也能治病?是的,「粪便疗法」药物已获批上市!

上一篇文章,我们为大家介绍了微生物群疗法开发的最前沿情况,包括艰难梭菌的介绍、感染艰难梭菌的症状与人群特征,以及治疗艰难梭菌感染的困境。
本文将继续为大家介绍首次批准使用人类粪便中微生物群药物的研发背景及疗效。
▲ 艰难梭菌的示意图
在艰难梭菌感染的治疗出现困境后,如何寻找一种行之有效的改善肠道环境的医疗方法是亟需解决的问题。
而“粪便移植”是打破艰难梭菌感染反复复发恶性循环的一种尝试。

“粪便移植”治疗
这种治疗方法是通过将肠道菌群处于平衡状态的健康人的粪便移植到患者体内,来恢复被抗菌素破坏的肠道菌群平衡。这是因为大量的肠道细菌随粪便排出,所以肠道菌群一定程度上可以在粪便中得以重现。
据说肠道细菌有1000多种,约100万亿个,但由于总体情况仍属未知,即使知道肠道菌群失衡,但目前尚无法找出需要补充的细菌,因此整体移植肠道菌群可以说是一种改善肠道环境的解决方法。

“粪便移植”疗效
粪便移植对艰难梭菌感染患者的有效性于2013年首次发表。来自荷兰阿姆斯特丹大学的一个研究团队在医学杂志《新英格兰医学杂志》上发表了研究结果。
研究团队将感染的患者分为三组,并研究他们在感染后10周内有无复发。第一组患者服用抗菌素四天后进行肠道清洁,再进行粪便移植;第二组患者服用抗菌素两周;第三组患者服用抗菌素两周后进行肠道清洁。
在接受1~2次粪便移植的一组中,无复发的患者比例为93.8%,而抗菌素组为31%,抗菌素和肠道清洁组为23%。
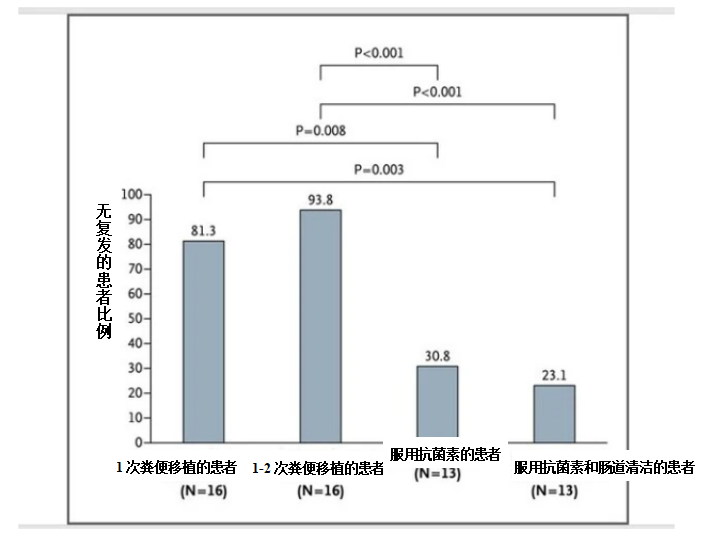
▲ 源自《新英格兰医学杂志》「Duodenal Infusion of Donor FeCes for ReCurrent Clostridium diffiCile」(2013年)
对7名接受粪便移植的患者在移植前和移植后14天的粪便以及移植捐赠者的粪便进行分析,针对肠内菌群的多样性进行了研究,结果显示,移植前多样性很差的患者的肠道菌群,在移植后变得与捐赠者的多样性大致相同。
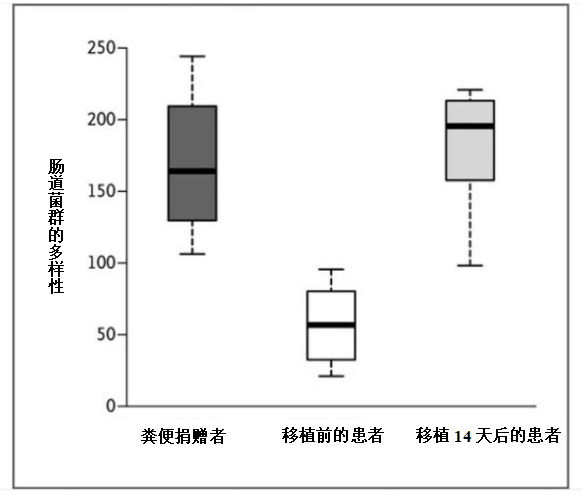
▲源自《新英格兰医学杂志》「Duodenal Infusion of Donor FeCes for ReCurrent Clostridium diffiCile」(2013年)
由于该报告的发表,从2013年起,在欧美粪便移植被广泛用于复发性艰难梭菌感染的治疗及预防。多项临床研究表明,该方法疗效显著。因此,包括2021年发布的美国消化系疾病学会指南在内的多项指南均推荐以粪便移植治疗复发性艰难梭菌感染。
上述的荷兰研究团队使用捐赠的粪便并在当天进行移植,但由于能够以这种方法进行移植的患者及医院有限,因此建立了一个粪便库,提前采集粪便并进行冷冻保存。

相关制剂开发及疗效
一些公司从2013年左右开始进行研究和开发,目的是开发一种安全有效、可以标准化稳定生产、并可获得FDA批准的制剂。
历经各种困难,包括难以招募临床试验参与者,目前瑞士Ferring公司的Rebyota第一个获得了批准。该产品最初是由Ferring公司收购的一家美国风投公司开发的,该公司自2013年以来一直在进行临床研究。
FDA对在美国和加拿大进行的一项最具科学可靠性的Rebyota双盲对照临床试验、以及另一项其它类型的临床试验进行了评价,发现在给药8周内,艰难梭菌感染未复发者的比例在Rebyota治疗组中为70.6%,而在安慰剂组中为57.5%。据Ferring公司称,在给药两个月内未见复发的人中,90%以上在六个月后也未复发。
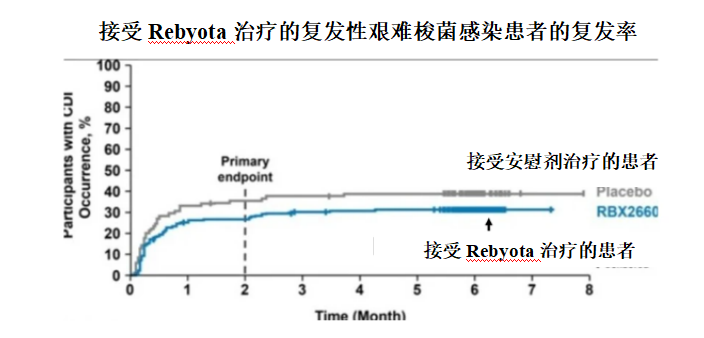
▲源自医学杂志《Drugs》「EfCaCy and Safety of RBX2660 in PUNCH CD3, a Phase III, Randomized,DoubleBlind, PlaCeboControlled Trial with a Bayesian Primary Analysis for the Prevention of ReCurrent Clostridioides difCile InfeCtion」(2022年)
在同一临床试验中,最常见的不良反应为腹痛,在接受Rebyota治疗的患者中,发生率为8.9%,发生频率高于安慰剂组的6.9%。其次,较常见的不良反应为腹泻(7.2%,而安慰剂组为3.4%)。
根据FDA的统计,临床试验中大多数的不良反应发生在用药后的两周之内,且大多数症状在用药后四周内缓解。在临床试验中未见致死不良反应。

Rebyota获批上市
然而,在批准该产品时,FDA指出,由于制剂是由人类粪便制成,即使事先进行病原体检测,也“可能会含有感染性病原体”,并且警告称,“目前尚不清楚该产品是否含有可能引发食物过敏的物质”。
在2021年9月FDA批准之前举行的咨询会议上,有人指出与安慰剂相比,Rebyota的效果并不是很大。然而,许多委员会成员建议FDA批准Rebyota,因为“鉴于复发性艰难梭菌患者缺乏理想的治疗方法,特别是对于三次或以上复发的患者,即使有中等程度的效果对这些患者来说也具有重大的意义”。
FDA负责人认为,Rebyota的批准是一个“重要的里程碑”,未来可能会出现更多基于微生物群的制剂。

仅就复发性艰难梭菌感染而言,已完成Ⅲ期临床试验的、或有望2023年底前完成最终临床试验的制剂,仅是美国就有两种。
与Rebyota不同的是,这两种制剂均是含有来源于粪便的细菌菌群的口服胶囊制剂。

持续研发
截至2023年4月18日,在美国政府运营的世界最大的临床试验数据库“ClinicalTrials.gov”中,登记有来自世界各地的3043项与微生物群相关的临床试验,其中不包括那些尚未开始招募参与者或已经停止的试验。
在日本,目前处理与人类共生的细菌菌群(包括肠道菌群)的主流方法是通过饮食等进行“肠道功能激活”。
未来,对于患有更严重症状的人,治疗方法可能会比肠道功能激活更进一步,将越来越多地使用含有细菌菌群的生物制剂。
更多前沿医疗内容,欢迎持续关注我们!如果您想了解更多专业信息,欢迎添加惠潆生命健康客服微信咨询。

欢迎咨询
请在备注中输入:230727

往 期 推 荐
|
|||
|
|||
|
关 于 惠 潆 生 命 健 康
惠潆生命健康H.Y Care专注于全方位的赴日医疗服务,布局海外医疗多年,拥有在日本注册的专业医疗公司及专业资质的医疗服务团队。公司位于东京高档商务区惠比寿,长驻日本的专职团队中80%为日籍员工。
公司长期深耕医药医疗领域,行业资源深厚,产业布局完善,与多家日本医药龙头企业和世界500强企业合作,依托清华大学和中科院生物所前沿生物医药科学资源,是清华校友聚投企业。
作为专业赴日医疗服务机构,我们能为您和您的家族成员,提供大病医疗、精密体检、抗衰养护、特色轻医美、辅助生殖、远程医疗咨询等全生命周期服务,满足中高端客户追求优质服务的需求。
同时,我们与日本大多数顶级医院达成官方战略合作关系,整合了日本各医疗领域里众多权威的公立、私立医疗机构和专家医生,其中包括为日本皇室家族服务的医生团队。
公司拥有日本医疗身元保证资质和旅游业资质及专业的医疗翻译人员,可根据客户需求提供一站式、个性化的贴心服务,保障客户出国看病期间的一切合法权益。
更专注,才安心,H.Y Care——您尊享贴心的赴日医疗服务专家。